Jesús Bosque Martínez1
Universidad Politécnica de Madrid,
ETSI Agronómica, Alimentaria y de Biosistemas,
Avda. Puerta de Hierro, 2,
28040 Madrid
- Imagen PET
- Una medida interesante
- Valor pronóstico del NHOC
- El origen de la inspiración
- Resolución numérica de la ecuación
- Simulaciones de crecimiento tumoral
- Conclusión
Agradecimientos
Bibliografía
En el contexto de la oncología es útil establecer modelos que permitan entender mejor el crecimiento del cáncer y cómo este responde a las distintas terapias. Gracias a esto pueden proponerse por ejemplo protocolos de tratamiento que obtengan la máxima efectividad del tratamiento. También pueden utilizarse estos modelos para proponer hipótesis que, tras ser validadas en la realidad, permitan definir marcadores cuantitativos que nos den información adicional del estado de la enfermedad. Para que esto funcione resulta fundamental que los modelos que se realizan se pongan en diálogo con los datos existentes procedentes de pacientes con cáncer.
Las matemáticas nos permiten establecer relaciones entre variables que suceden en procesos del mundo real, cuantificarlas, y estudiar cómo esas relaciones modifican el sistema. A partir de ello podemos saber cómo este sistema evoluciona, o cómo cambia ante condiciones diferentes. A este tipo de abstracción matemática se la conoce como modelo matemático. Los modelos son versiones simplificadas de la realidad, pero incorporan los elementos fundamentales que influyen en un cierto fenómeno. Su utilidad es que pueden analizarse mediante métodos matemáticos para extraer más información de la que da el propio sistema, o bien simularse en un ordenador.
En este artículo describiremos un caso particular de aplicación de modelado matemático del cáncer y su aprovechamiento conjunto con datos de pacientes para ampliar nuestro conocimiento de la enfermedad. Nuestro resultado en este caso es un biomarcador de imagen, es decir, una variable que podemos medir en las imágenes que se toman durante el diagnóstico de los pacientes y que sirve para predecir cuánto de agresivo será un caso particular [1].
1. Imagen PET
Cuando un paciente es diagnosticado de cáncer habitualmente se le somete a una prueba de imagen conocida como tomografía por emisión de positrones (PET). Esta técnica es un tipo de imagen metabólica, porque permite visualizar los procesos metabólicos que existen en las células [2]. Para tomar una imagen PET se comienza por inyectar en el cuerpo del paciente una sustancia análoga a la glucosa llamada FDG que tiene adherido un isótopo radiactivo (flúor {}^{18}\mathrm{F}). Esta glucosa modificada se distribuye por el cuerpo del paciente a través de la sangre y se dirige a las zonas que tienen un consumo preferente de la sustancia. Una de estas zonas son los tumores malignos, que tienen una gran avidez de glucosa debido a que la utilizan para mantener activos sus procesos de proliferación.
Después de un tiempo breve, los isótopos radiactivos que están adheridos a la FDG se descomponen y cada uno de ellos emite una partícula subatómica que se conoce con el nombre de positrón. Los positrones emitidos interaccionan con la materia circundante generando una señal que puede detectarse en un tomógrafo en el que está colocado el paciente. Esta señal se utiliza entonces para reconstruir de manera precisa los lugares en los que se ha emitido y cuánto de intensa ha sido la emisión, lo que es proporcional a cuánta glucosa había en una zona en particular. El resultado se traduce en una imagen tridimensional en escala de grises, que visualiza qué zonas internas del cuerpo están consumiendo glucosa y en qué medida. Cuanto más negro se ve, mayor es el consumo. En la siguiente imagen (Figura 1) se aprecia un corte concreto (la imagen completa es en 3D) de un estudio PET en un paciente con cáncer de pulmón.
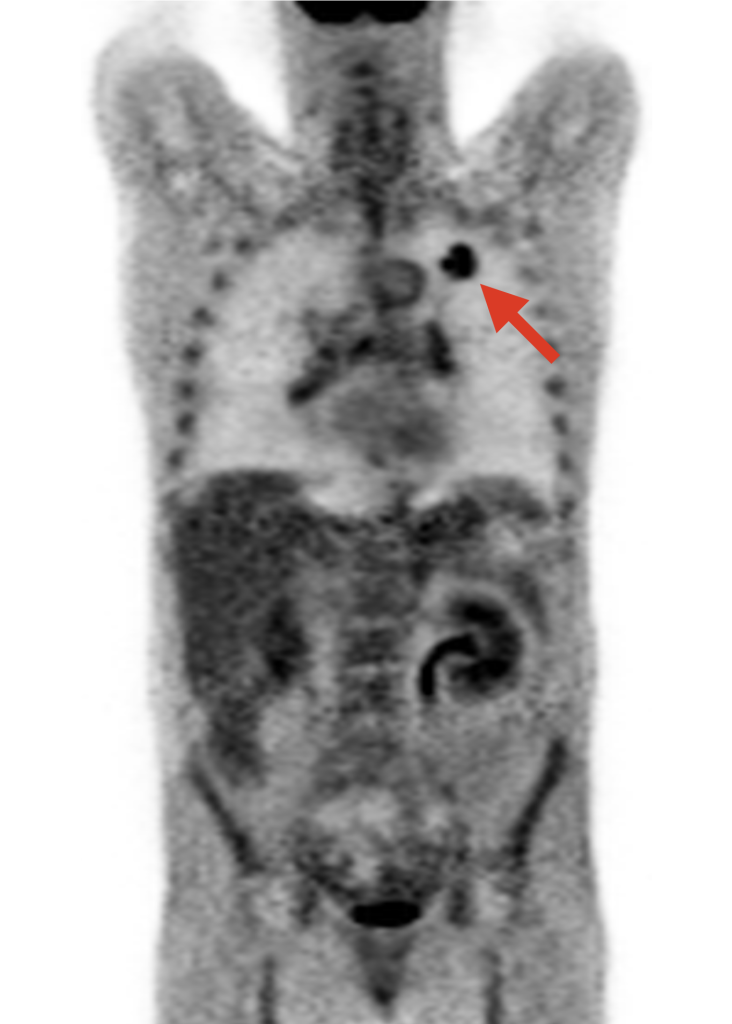
En estas imágenes el tumor se visualiza claramente, lo cual es muy útil para los médicos. Lo interesante para los matemáticos es que estas imágenes contienen datos estructurados espacialmente que informan de qué zonas del tumor están consumiendo más o menos glucosa y dónde se encuentran localizadas (Figura 2). El nivel de escala de gris que se visualiza en la imagen representa normalmente una medida de consumo de glucosa que se llama Standardized Uptake Value (SUV). Zonas con alto SUV corresponden a zonas de alta absorción de glucosa (correspondientes, como hemos dicho, a zonas con gran proliferación celular) y se visualizan de color negro. De manera correspondiente, zonas blancas o con gris muy suave son zonas en las que no hay gran captación (bajo SUV). En general, encontramos que distintas zonas del tumor tienen distintos niveles de captación, ya que el cáncer es una enfermedad muy heterogénea.

Desde un punto de vista matemático, la imagen es una matriz en 3D que contiene los valores de SUV localizados en el espacio. Una imagen en 2D tiene un valor asociado a cada píxel, regiones cuadradas en las que se divide el espacio; nuestra imagen en 3D por su parte está divida en vóxeles, que son las regiones del mismo tamaño con forma de prisma cuadrangular en las que se divide el espacio. Cada uno de estos vóxeles tridimensionales tiene asociado un valor de SUV.
Una vez que tenemos la imagen del paciente, debemos seleccionar en ella la región donde se visualiza el tumor. A continuación segmentamos esta región, es decir, contorneamos la extensión del tumor en la imagen para quedarnos exclusivamente con esta región de interés (línea verde en la figura 2). Sobre esta matriz de valores podemos hacer infinidad de cálculos matemáticos que nos informan del estado del metabolismo tumoral. A este proceso en numerosas ocasiones se lo conoce con el término radiómica [3].
2. Una medida interesante
Algunas de las medidas que se extraen de las imágenes PET (y de otros tipos de imagen médica) pueden utilizarse para predecir cómo evolucionará la enfermedad del paciente y qué pacientes están asociados a un mayor riesgo. Es decir, podemos utilizar esta información para efectuar un pronóstico del paciente. Esto es de gran importancia para poder identificar casos de especial gravedad y tratarlos de manera personalizada.
Una medida de este estilo es el valor de la máxima actividad metabólica que se aprecia en ella, variable conocida como SUVmax. Esta variable sencilla nos informa de cuánto de alta es la actividad en un tumor determinado, lo cual está muy relacionado con la agresividad de este tumor: a mayor actividad metabólica, mayor agresividad.
Dado que este valor es tan relevante, nos preguntamos si su posición en el conjunto del tumor estaría también relacionada con su agresividad. Para evaluarlo localizamos espacialmente este punto con respecto a la referencia del centro del tumor. Como representante de este último utilizamos el centroide correspondiente a su forma geométrica, es decir, la posición promedio en cada una de las 3 direcciones del espacio de todos los N vóxeles del tumor:
\mathbf{x}^c=\frac{\mathbf{x}_1+\cdots+\mathbf{x}_N}{N}.\qquad (1)
¿Está el punto donde se alcanza SUVmax cerca o lejos de este centroide? Para saberlo únicamente tenemos que computar la distancia euclídea entre los dos puntos. Denominamos a esta distancia HOC (distance from the metabolic hotspot to the tumor centroid ) y la calculamos según las coordenadas espaciales de los dos puntos implicados como
donde \mathbf{x}^M es el vector de posición del vóxel en el que se alcanza el valor SUVmax. Recordemos que un vector \mathbf{x} en el espacio tiene tres coordenadas, \mathbf{x}=(x,y,z). En la figura 3 puedes ver una visualización de esta medida.
Esencialmente, el HOC nos dice la distancia que separa el vóxel con SUVmax del centroide geométrico del tumor. Si esta distancia es muy pequeña, ambos puntos estarán muy cercanos. Si es muy grande, el punto con más actividad metabólica estará situado lejos del centro.

Sin embargo, más allá de la distancia como tal, nos gustaría disponer de una medida que fuese independiente del tamaño del tumor y nos permitiese comparar tumores con diferentes volúmenes. Para ello normalizamos el HOC por una medida del tamaño tumoral. Normalizar significa dividirlo por una medida que cuantifique dicho tamaño con el objetivo de obtener una variable adimensional que pueda compararse entre distintos tumores independientemente de su tamaño.
Una medida lineal que podemos usar para efectuar esta normalización es el radio medio esférico (MSR), radio que correspondería al volumen del tumor si este tuviese forma esférica. No es difícil partir de la fórmula del volumen V de una esfera de radio R,
V=\frac{4\pi}{3}R^3,para despejar el radio que corresponde a un volumen determinado:
\mathrm{MSR} =\sqrt[3]{\frac{3}{4\pi}V}.Finalmente, para obtener la posición normalizada del vóxel con SUVmax, a la que llamaremos NHOC (normalized distance from hotspot to centroid), simplemente dividimos HOC entre MSR:
\mathrm{NHOC} = \frac{\mathrm{HOC}}{\mathrm{MSR}}.Esta medida final normalizada nos informa de dónde se localiza la máxima actividad con respecto al centro del tumor y es muy fácil de interpretar. Si el NHOC es 0 significa que la máxima actividad se localiza exactamente en el centro. Por el contrario, valores del NHOC cercanos a 1 indican que el consumo metabólico más alto está cercano al borde del tumor (Figura 4).
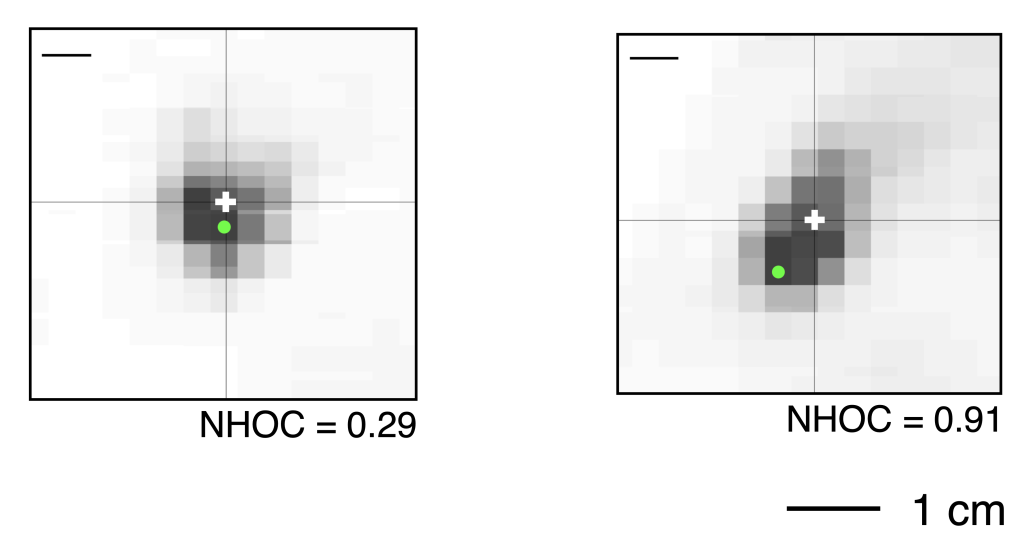
3. Valor pronóstico del NHOC
Calculamos esta distancia en las imágenes PET de diagnóstico de un número elevado de pacientes que habían padecido cáncer de pulmón o cáncer de mama en el pasado. Estos pacientes, bien se habían recuperado o habían fallecido o, como última opción, estaban todavía luchando con la enfermedad. El tiempo de supervivencia formaba también parte del estudio, de manera que contábamos con la información de cuánto tiempo había pasado desde el momento del diagnóstico hasta el fallecimiento del paciente o cuánto tiempo había sobrevivido hasta el tiempo actual.
Encontramos que había grandes diferencias entre los valores de NHOC de distintos pacientes, con pacientes con NHOC muy pequeños y otros con NHOC altos. La pregunta que nos hicimos fue si estas diferencias de NHOC estaban asociadas a la supervivencia de los pacientes a la enfermedad. En otras palabras, la pregunta es si pacientes con NHOC bajo tenían más (o menos) probabilidades de sobrevivir a la enfermedad que los pacientes con NHOC alto.
Para responder a esta pregunta dividimos los dos grupos de pacientes (cáncer de pulmón y cáncer de mama) en dos subgrupos cada uno: aquellos que tenían un NHOC más bajo que un umbral dado y aquellos que tenían un NHOC más alto. En los dos tipos de cáncer encontramos que los pacientes con NHOC bajo tenían una supervivencia mucho mayor [1].
En el caso de cáncer de pulmón, dado que este grupo de pacientes estaba compuesto por tumores operables, muchos pacientes habían sobrevivido al tratamiento. Pese a ello, alrededor del 60 % de los pacientes de este grupo había fallecido después de un tiempo de unos 8 años. Lo interesante de los resultados es que la diferencia entre el tiempo que habían sobrevivido los pacientes con NHOC alto y el de los pacientes con NHOC bajo era muy grande. En el grupo de NHOC alto la supervivencia mediana, es decir, el tiempo que sobrevive la mitad de la población, era de únicamente dos años y medio. Por contra, los pacientes con NHOC bajo tenían una supervivencia mediana de más de siete años, una diferencia de casi 5 años.
Las pacientes con cáncer de mama mostraban en este caso una mortalidad muy baja. Únicamente un 10 % de las pacientes de este grupo fallecían. Lo que resulta sorprendente es que ninguna de las pacientes que tenían un NHOC bajo fallecieron, encontrándose todas las que sí lo hacían en el grupo de NHOC alto. Es decir, la variable NHOC nos permitía emitir un pronóstico y señalar aquellas pacientes que tenían mayor riesgo. Esto no significa que tener un NHOC alto en el momento del diagnóstico implique que la paciente no sobrevivirá, pero sí permite distinguir de manera previa qué pacientes se beneficiarán de una enfermedad más indolente.
En definitiva, el NHOC permite dar un pronóstico más preciso de los pacientes, ya que un NHOC alto se asocia, en promedio, a una peor supervivencia a la enfermedad.
4. El origen de la inspiración
Pero, ¿qué fue lo que nos llevó a pensar que la posición del punto de máxima actividad podía estar relacionada con el pronóstico de los pacientes? Para responder a esta pregunta tenemos que presentar un modelo matemático de crecimiento tumoral con el que estábamos trabajando en aquel momento.
El modelo se conoce como ecuación de Fisher-Kolmogorov y lleva el nombre de dos gigantes de la Matemática del siglo XX (Figura 5) [4, 5]. Se trata de un modelo “de juguete”. Esto quiere decir que reproduce algunas características básicas del crecimiento tumoral, pero lo hace de manera muy simplificada. Sirve para entender cómo progresa la enfermedad de manera cualitativa, pero no puede considerarse que sus resultados sean fieles al comportamiento exacto del tumor. Es simplemente una aproximación útil.

La ecuación de Fisher-Kolmogorov describe la evolución en el tiempo y en el espacio de una variable u de densidad celular, es decir, el número de células que encontramos por unidad de volumen en cada punto del espacio. Esta densidad es por tanto una función de varias variables: el tiempo t y la posición en el espacio \mathbf{x}, lo que escribimos como u(\mathbf{x}, t). Es posible que hasta el momento únicamente hayas estudiado funciones f(x) de una única variable; aquí el concepto es el mismo, pero considerando que esta densidad depende de 4 variables: el tiempo y cada una de las direcciones del espacio.
Para definir su evolución temporal igualamos su tasa de cambio en el tiempo (su derivada respecto al tiempo) a la suma de los dos términos implicados que producen esta variación. En este caso hay dos procesos básicos de las células: proliferación (es decir, dividirse para dar lugar a nuevas células) y migración (moverse en el espacio).
El primer término, el de proliferación, lo describimos a través de la llamada función logística. Esta función indica que las células que se dividen dependen de manera lineal del espacio disponible: cuantas más células haya en un cierto punto, menor será la proliferación de estas células porque no habrá espacio disponible para ello. Matemáticamente lo escribimos como
\mathrm{proliferación} = \rho u \left(1 − \frac{u}{K}\right),recordando que u es la densidad celular. El parámetro \rho modula cuánto proliferan las células que estamos estudiando, mientras que K indica cuál es la densidad de células máximas que puede haber en un punto del espacio.
Por otro lado, para escribir el término de migración se asume que las células se mueven de manera aleatoria en todas las direcciones del espacio por igual. Aunque esto no sucede exactamente así, es una primera aproximación muy útil, entre otras cosas, porque esta es la manera en la que se mueven los átomos de un gas y conocemos bien la ecuación que rige este movimiento:
\mathrm{migración} = D\nabla^2u.Aquí el operador \nabla^2 aplicado a una función que depende de varias variables se conoce como Laplaciano e indica la suma de las derivadas de segundo orden con respecto a las variables espaciales. Así queda \nabla^2u = \frac{\partial^2u}{\partial x^2} + \frac{\partial^2u}{\partial y^2} + \frac{\partial^2u}{\partial z^2}. Puedes interpretar el signo \partial como el de las derivadas habituales que conoces, con la diferencia de que utilizamos este signo (derivada parcial) cuando tenemos más de una variable independiente. El parámetro D simplemente nos informa de cuánto de veloz es ese movimiento de las células.
Aunque esta expresión para la migración supera las matemáticas que se estudian en bachillerato, hay una interpretación intuitiva que puede hacerse. Si todas las células se están moviendo aleatoriamente en el espacio, habrá muchas células que se moverán desde un lugar muy ocupado hacia otro con menos densidad, mientras que habrá pocas que se muevan desde puntos con baja densidad hacia los muy ocupados. Por lo tanto, si un punto tiene más densidad que su entorno, las células tienden a salir de este punto y viceversa. En consecuencia, el movimiento de células en cada instante tenderá poco a poco a promediar la densidad que hay en un cierto punto con la de los puntos que tiene alrededor.
En definitiva, la ecuación completa (Fisher-Kolmogorov) que modela el crecimiento tumoral es
\frac{\partial u}{\partial t} = \mathrm{migración} + \mathrm{proliferación} = D\nabla^2u + \rho u \left(1 − \frac{u}{K}\right).Lo que esta ecuación nos dice es que, en cada punto del espacio, la tasa de cambio en el tiempo (término izquierdo) corresponde al número de células nuevas que aparecen (proliferación) más las que llegan desde puntos cercanos (migración).
Esto es una ejemplo de ecuación diferencial, un tipo muy importante de ecuación que tiene por solución una función y se escribe a partir de la lógica que rige el comportamiento puntual. Por ejemplo, en este caso, a partir de saber cómo varía la densidad celular en un cierto instante (derivada temporal) según el espacio disponible, que rige la proliferación, y la ocupación del entorno, que rige la migración. Este caso particular es una ecuación en derivadas parciales, ya que la función incógnita depende de varias variables (las espaciales y el tiempo).
Para poder resolver una ecuación de este estilo necesitamos en primer lugar conocer cuál es el estado inicial de su incógnita (en este caso la densidad celular), lo que se conoce como condición inicial. En este caso, consideraremos un número inicial muy pequeño de células que se sitúa en el centro. También necesitamos saber cómo se comportan los extremos (condiciones de contorno), aunque esas particularidades superan el alcance de este artículo.
5. Resolución numérica de la ecuación
Muchas ecuaciones como la anterior son difíciles o imposibles de resolver de manera analítica y por ello recurrimos a un ordenador para resolverlas de manera aproximada utilizando los valores de la función en puntos discretos, lo que se conoce como solución numérica [6]. Para simplificarlo, vamos a considerar que el tumor crece igual en todas las direcciones del espacio, de manera que utilizaremos únicamente la dirección radial como variable espacial. Pasamos entonces de tener 3 direcciones del espacio a quedarnos con una sola que representa la distancia radial desde el origen de coordenadas.
El siguiente paso consiste en dividir el espacio en una serie de puntos discretos separados un cierta distancia. En lugar de usar la función completa en todo su dominio, sólo vamos a trabajar con su valor aproximado en cada uno de estos puntos. A continuación, entenderemos que la derivada temporal nos dice cuánto cambia cada punto entre un instante y el siguiente. Además, esta derivada la podemos evaluar, porque disponemos de la información del lado derecho de la ecuación.
Comenzando por la condición inicial iremos actualizando el estado en pasos discretos de tiempo. En cada instante aproximamos el valor de la derivada temporal según el valor que tengan los términos de proliferación y migración, los cuales, como sabemos, dependen de cuál sea la ocupación en cada punto del espacio y de cuál sea la ocupación con respecto a sus vecinos, respectivamente.
La actualización de este estado en cada tiempo nos informa de cómo va cambiando la función incógnita y nos permite ir actualizándola en el instante siguiente, resolviendo así de forma aproximada la ecuación. Este método de resolución se conoce con el nombre de diferencias finitas y da una aproximación numérica de la solución u(\mathbf{x}, t). Esto implica que lo que vamos a tener son los valores discretos que toma u en puntos discretos de espacio y tiempo, en lugar de una expresión matemática completa para la función.
6. Simulaciones de crecimiento tumoral
Gracias al método anterior podemos por tanto simular de manera simplificada cómo crece un tumor a partir de la ecuación de Fisher-Kolmogorov.
Al visualizarlo (Figura 6) vemos en azul la curva que representa la solución de la ecuación u(r, t), es decir, la densidad de células que tenemos en cada punto radial a una cierta distancia r del centro. La representación tridimensional de la derecha simplemente visualiza un número determinado de células proporcional a la densidad en regiones del espacio para ilustrar lo ocupadas que están estas.
Inicialmente tenemos una densidad muy baja, que se encuentra fundamentalmente localizada en el centro (Figura 6, 180 días). Según el tiempo avanza, esta densidad va creciendo y ocupando más y más esta zona central hasta que, en un momento dado, el espacio en esta zona queda copado. Las células se ven entonces obligadas a ocupar progresivamente el tejido adyacente: el tumor ha saturado el espacio y va desplazándose hacia radios mayores (Figura 6, a partir de 260 días).
Por otro lado, la curva roja representa el perfil proliferativo de este tumor teórico, es decir, la evaluación del término de proliferación en cada radio. Esta curva nos dice cuántas células nuevas están apareciendo en cada lugar. Vemos cómo al principio la mayor parte de las células se crean en el centro, porque es donde más células hay y donde todavía hay espacio disponible (Figura 6, 180 días). Sin embargo al saturarse el centro las células no pueden proliferar más en esa zona y el pico de la curva roja se mueve a zonas donde hay más espacio y, por tanto, más células proliferando (Figura 6, 260 días en adelante). Las simulaciones permiten observar que este perfil proliferativo inicialmente se encuentra centrado en el tumor, pero progresivamente se aleja de este centro (ver por ejemplo la diferencia entre 320 días y 650 días en la figura 6).
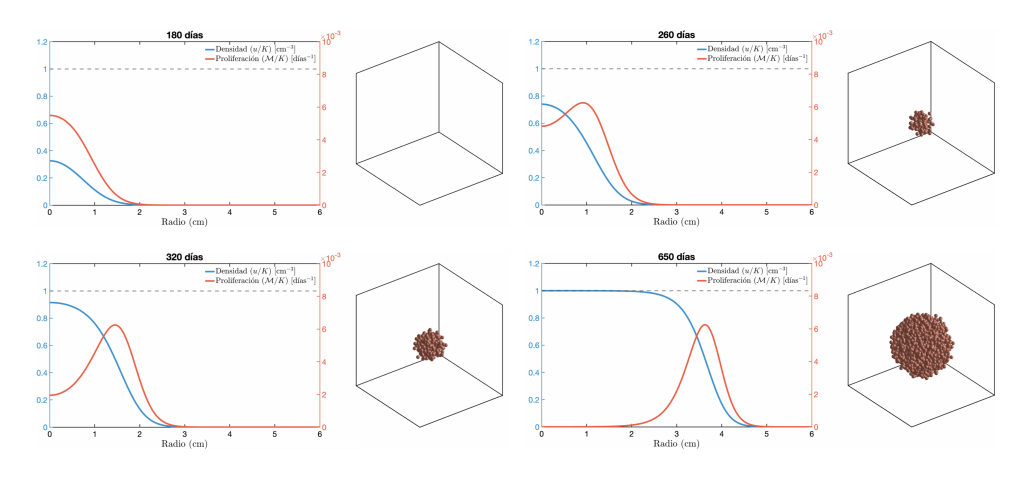
Podemos interpretar estas simulaciones en términos de HOC. Tendremos entonces que localizar dónde se encuentra el punto de máxima actividad proliferativa (el máximo de la curva roja) y ver cuán lejos está del centro. Las simulaciones nos indican que esta distancia crece según el tiempo avanza y el tumor progresa.
Por otro lado, el NHOC nos informa de la distancia normalizada con respecto al tamaño del tumor. En un principio, cuando la actividad está localizada en el centro, el NHOC es 0. Cuando el centro se ha llenado, el punto más activo se desplaza hacia la derecha y el NHOC comienza progresivamente a aumentar. Finalmente, en un estado muy avanzado el punto de máxima proliferación se situará muy cerca del borde del tumor y el NHOC será muy cercano a 1.
Así pues las simulaciones sugieren que el NHOC crece según el tumor alcanza estados más avanzados, comenzando en 0 para tumores muy iniciales y llegando a un valor cercano a 1 cuando el tumor está muy avanzado. Tumores más avanzados tendrán por tanto un mayor valor de NHOC. Esta es la idea que generó la intuición, que trasladamos a imagen PET de pacientes como indicador de proliferación y que resultó ser exitoso para predecir su supervivencia.
7. Conclusión
En este artículo hemos descrito un aplicación real de cómo el modelado matemático, incluso cuando no pretende ser preciso, es muy útil para entender un sistema y desvelar parámetros clave de su comportamiento.
A partir de simulaciones de un modelo simplificado de crecimiento tumoral pudimos identificar el patrón que indicaba que la máxima actividad proliferativa debía situarse progresivamente lejos del centro a medida que el tumor avanzaba. Posteriormente trasladamos esta concepción a las imágenes PET de los pacientes y comprobamos que efectivamente aquellos que mostraban la máxima actividad desplazada del centro estaban asociados a una menor supervivencia. Este hecho nos permite entonces definir la distancia normalizada NHOC como un biomarcador de imagen con utilidad en la medicina personalizada.
El uso conjunto del modelado matemático y el análisis avanzando de datos de pacientes permite mejorar el conocimiento de la enfermedad, resaltando el importante papel que juegan las matemáticas en la ciencia actual.
Agradecimientos
Agradezco a los coautores de esta investigación [1], que fue producto de un verdadero trabajo en equipo.
Bibliografía
[1] Juan Jiménez-Sánchez, Jesús J. Bosque, Germán A. Jiménez Londoño, David Molina-García, Álvaro Martínez, Julián Pérez-Beteta, Carmen Ortega-Sabater, Antonio F. Honguero Martínez, Ana M. García Vicente, Gabriel F. Calvo, and Víctor M. Pérez-García. Evolutionary dynamics at the tumor edge reveal metabolic imaging biomarkers. Proceedings of the National Academy of Sciences 118(6):e2018110118, 2021. J.J.-S. and J.J.B. contributed equally to this work.
[2] Gary A. Ulaner. Fundamentos de la PET-TC en oncología. Elsevier Health Sciences, 2020.
[3] Philippe Lambin, Emmanuel Rios-Velazquez, Ralph Leijenaar, Sara Carvalho, Ruud GPM Van Stiphout, Patrick Granton, Catharina ML Zegers, Robert Gillies, Ronald Boellard, André Dekker, et al. Radiomics: extracting more information from medical images using advanced feature analysis. European journal of cancer 48(4):441–446, 2012.
[4] Ronald Fisher. The wave of advance of advantageous genes. Annals of eugenics 7(4):355–369, 1937.
[5] Andrey N. Kolmogorov, Ivan G. Petrovskii, and Nikolai S. Piskunov. Study of the diffusion equation with growth of the quantity of matter and its application to a biological problem. Bulletin of Moscow University, Mathematics and Mechanics 1:1–25, 1937.
[6] Richard L. Burden, Jesús Ildefonso Díaz Díaz, J. Douglas Faires, Rafael Iriarte Balderrama, and Francisco Paniagua Bocanegra. Análisis numérico. México: Grupo Editorial Iberoamérica, 1996.
- jesus.bosque@upm.es ↩︎